![]()
حسگرهای شیمیایی
یک حسگر شیمیایی وسیله ای است که اطلاعات پیوسته ای را در مورد خواص شیمیایی محیط اطرافش در اختیار می گذارد. یک حسگر
شیمیایی پاسخ خاصی را که به طور مستقیم با کمیت گونه شیمیایی به خصوصی مربوط است، تولید می کند.
حسگرهای شیمیایی دارای یک عنصر انتقال دهنده علائم، پوشیده از یک لایه شناساگر شیمیایی یا زیستی می باشند.
این لایه با ترکیب موردنظر وارد واکنش می شود و تغییرات شیمیایی به وجود آمده از این بر هم کنش را توسط عنصر انتقال دهنده به علائم
الکتریکی تبدیل می کند.
حسگرهای شیمیایی به چهار دسته تقسیم می شوند.
- حسگرهای الکتریکی
- حسگرهای نوری
- حسگرهای گرمایی
- حسگرهای جرمی
حسگرهای الکتروشیمیایی
حسگرهای الکتروشیمیایی (الکتریکی) زیر شاخه مهمی از حسگرهای شیمیایی را به وجود می آورند. در این نوع حسگرها، الکترود به عنوان
عنصر انتقال دهنده علائم مورد استفاده قرار می گیرد. چنین ابزارهایی در حال حاضر از موقعیت برجسته ای در میان حسگرهای موجود
برخوردارند و به مرحله تجاری رسیده اند.
حسگرهای الکتروشیمیایی به سه دسته تقسیم می شوند :
- حسگرهای پتانسیومتری
- حسگرهای آمپرومتری
- حسگرهای هدایت سنجی
حسگرهای پتانسیومتری
حسگرهای پتانسیومتری، گسترده ترین گروه حسگرهای الکتروشیمیایی هستند. آن ها ابزاری هستند که پتانسیل خوانده شده توسط آن ها،
به طور خطی با لگاریتم فعالیت یون مورد اندازه گیری در محلول رابطه دارد. این دسته از حسگرها، بسیار ارزان و ساده می باشند و از اوایل دهه
۱۹۳۰ به طور کاربردی مورد استفاده قرار گرفته اند.
این حسگرها به چهار گروه تقسیم می شوند که هر یک مکانیسم عمل متفاوتی دارند.
- الکترودهای یون گزین (ISE)
- الکترودهای سیم روکش دار (CWE)
- الکترودهای حالت جامد
- ترانزیستور با اثر میدان (FET)
الکترودهای یون گزین
الکترودهای یون گزین، مهمترین و کاربردی ترین گروه از این دسته هستند. الکترودهای یون گزین برای بیشتر آنالیت ها در گستره وسیعی از
غلظت، وابستگی خطی نشان می دهند. الکترودهای یون گزین نمونه ها را از بین نمی برند، آلودگی بسیار کمی ایجاد می کنند و زمان پاسخ آن
ها معمولاً کوتاه است. از این رو می توان از آن ها در کاربردهای کلینیکی استفاده نمود. این الکترودها قابلیت اندازه گیری محلول های خیلی کدر
و رنگی را دارند. همچنین الکترودهای طراحی شده ویژه را می توان در محیط هایی از قبیل سلول های زنده استفاده کرد.
از معایب اندازه گیری با الکترودهای یون گزین می توان به مزاحمت یون های همراه، اثر قدرت یونی محلول بر پاسخ الکترود، تثبیت دما و pH در
حین اندازه گیری ها اشاره کرد. الکترودهای یون گزین، غلظت یون های در حال تعادل در سطح را اندازه گیری می کنند.
در محلول های رقیق، غلظت مستقیماً در ارتباط با تعداد کل یون های موجود در محلول است. در غلظت های بالاتر، بر هم کنش بین یونی مانع
مهاجرت و رسیدن یون اولیه به سطح الکترود می شود، بنابراین پتانسیل اندازه گیری شده کمتر از حد انتظار است.
الکترود یون گزین، الکترود شناساگری است که می تواند به طور انتخابی فعالیت یک گونه یونی ویژه را اندازه گیری کند. چنین الکترودهایی پاسخ
سریع و گسترده خطی وسیعی را نشان می دهند که از رنگ یا کدورت محلول متأثر نمی شود. در ضمن موجب تخریب نمونه نشده و بسیار کم
هزینه می باشند. به طور مطلوب، پاسخ الکترود یون گزین باید از معادله نرنست (۱-۱) ، تبعیت کند.
E = K + (2.303RT / ZiF) log ai
که در این رابطه E پتانسیل، Zi و ai به ترتیب بار و فعالیت یونی می باشند. ثابت K شامل تمام پتانسیل های مستقل از نمونه می باشد. این
معادله پیشگویی می کند که نتیجه ده برابر تغییر در فعالیت یک یون، شیب پاسخ الکترود به صورت معنی دار ۵۹٫۱/Zi میلی ولت می باشد.
عبارت رفتار نرنستی برای چنین رفتاری به کار می رود. بر عکس، وقتی که شیب پاسخ الکترود به صورت معنی دارد کمتر از ۵۹٫۱/Zi میلی ولت
باشد، الکترود با یک رفتار زیر نرنستی مشخص می شود.
در الکترودهای یون گزین از فعالیت یون ها به جای غلظت آنها در محلول استفاده می کنند. عبارت فعالیت برای بیان غلظت مؤثر یون به کار می
رود. اختلاف بین غلظت و فعالیت به دلیل برهمکنش های یونی به وجود می آید. فعالیت یون I در محلول (ai)، با غلظت آن (Ci) از طریق معادله
(۱-۱) به دست می آید.
(۲-۱) ai = fi . Ci
که در این معادله fi ضریب فعالیت است. این ضریب تابع یون های موجود در محلول و قدرت یونی محلول می باشد. ضریب فعالیت با معادله دبای-
هوکل (۱-۳)، ارائه می شود :
![]()
(۳-۱)
که در آن μ قدرت یونی محلول است. بنابراین ضریب فعالیت در محلول های بسیار رقیق به یک نزدیک می شود. انحراف از یک، با افزایش بار یون
بیشتر می شود.
طبقه بندی الکترودهای یون گزین
بسته به طبیعت ماده به کار رفته شده در طراحی و ساخت یک الکترود، الکترودهای انتخابی یون به سه گروه الکترودهای با غشاء شیشه، مایع
و جامد تقسیم می شوند.
الکترودهای با غشاء شیشه
الکترودهای شیشه، پاسخگوی کاتیون های یک ظرفیتی می باشند. برگزیدگی برای کاتیون ها با تغییر ترکیب غشاء شیشه ای نازک و حساس به
یون حاصل می شود.
الکترودهای pH
الکترود pH به طور گسترده برای اندازه گیری pH در دهه های متعدد به کار رفته است. موفقیت چشم گیر الکترود pH به کارایی تجزیه ای،
انتخابگری زیاد برای یون های هیدروژن، گستره پاسخ دهی وسیع و پاسخ سریع و پایدار آن نسبت داده می شود. پدیده انتخابگری شیشه در
سال ۱۹۰۶ توسط کرمر گزارش شده است. الکترودهای شیشه pH، با آرایش و ابعاد مختلف، برای بیش از شش دهه از زمان ورود آن به بازار،
توسط بکمن کاربرد روزمره داشته اند. طرحی از یک آرایش الکترود شیشه pH، با کاربرد متداول در شکل ۱-۱ نشان داده شده است.
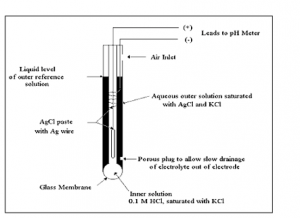
شکل (۱-۱): شمایی از یک الکترود pH مرکب
الکترودهای با غشاء مایع
الکترودهای انتخابگر از نوع غشاء مایع، مبتنی بر مواد مایع غیر قابل اختلاط با آب هستند که در درون غشاء پلیمری نفوذ داده شده اند.
این سنسورها نسبت به فعالیت یون هدف واکنش نشان داده و معمولاً محدوده حساسیت وسیعی را از حدود ۱ تا ۶-۱۰ مولار پوشش می دهد.
گزینش پذیری آنها به ثابت تعادل واکنش مبادله یون های هدف و مزاحم میان فازهای آلی و آبی مربوط می شود این گزینش پذیری به شدت به
نسبت ثابت تشکیل کمپلکس این یون ها و یونوفر موجود در فاز غشاء وابسته است.
این الکترودها به طور گسترده برای اندازه گیری های پتانسیومتری به کار می روند. این گونه الکترودهای انتخابگر یونی به دلیل اندازه گیری
مستقیم کاتیون های چند ظرفیتی متعدد و نیز برخی از آنیون ها حائز اهمیت می باشند. غشاء پلیمری (معمولاً ساخته شده از PVC پلاستیکی
شده) محلول آزمایشی را از بخش درونی که حاوی محلولی از یون مورد نظر است، جدا می کند. جزء فعال شناساگر غشاء ، یونوفر نام دارد.
یونوفرها در اشکال غیر پیچیده خود، باردار بوده و یا به لحاظ الکتریکی خنثی می باشند. نخستین یونوفرهای خنثی به کار رفته در غشاهای ISE،
آنتی بیوتیک ها بودند. پس از آن ها تعداد زیادی از حامل های خنثی و سنتتیک و عمدتاً بدون بار برای واکنش به کار گرفته شدند.
الکترودهای با غشاء جامد
این الکترودها، کاربردهای تجزیه ای فراوانی دارند. از میان انواع متنوع آن ها غالباً پلاتین، نقره، نیکل و مس مورد استفاده قرار می گیرند. پاسخ
این الکترودها به چگونگی سطح الکترود بستگی دارد. از این رو هنگام استفاده از این نوع الکترودها برای دستیابی به پاسخ تکرار پذیر، لازم است که سطح آن ها به خوبی صیقل داده شود.
کار قابل ملاحظه ای برای توسعۀ غشاهای جامد که اساساً برای آنیون انتخابی هستند، انجام گرفته است. غشاء حالت جامد می تواند از تک
بلورها، لایه های چند بلوری و یا مخلوط بلورها ساخته شود.
الکترودهای کربن
امروزه الکترودها بر پایه کربن در سطح وسیعی جهت تجزیه الکتروشیمیایی مورد استفاده قرار می گیرند. این امر به دلیل ارزان قیمت بودن،
سادگی تهیه، تجدید پذیری آسان سطح، بی اثری شیمیایی و مناسب بودن آن ها برای کاربردهای حسی و تشخیصی می باشد.
سرعت های انتقال الکترون مشاهده شده در سطوح کربنی، اغلب از سرعت های مشاهده شده در الکترودهای فلزی کمتر است. متداول ترین
انواع الکترودهای کربنی شامل کربن شیشه ای، الیاف کربنی، نانولوله های کربنی و خمیر کربن می باشند.
الکترود کربن شیشه ای
الکترود کربن شیشه ای، الکترودی بسیار محکم بوده و نسبت به گازها نفوذ ناپذیر می باشد. تکرار پذیری در خواص فیزیکی و شیمیایی این نوع
الکترودها که به روش های مختلف ساخته شده اند، متفاوت می باشد. بنابراین باید شرایط ساخت این گونه الکترودها را کنترل کرد تا
الکترودهایی با ساختار و فشردگی متفاوت حاصل شوند. این نوع الکترودهای جامد خواص مکانیکی و الکترونیکی خوبی دارند، از نظر شیمیایی
بی اثر می باشند و در روش های تجزیه ای، نسبتاً پاسخ های تکرارپذیری را ارائه می کنند.
ساختمان کربن شیشه ای، شامل نوارهای ظریف در هم پیچیده متشکل از صفحات شبه گرافیتی با اتصال عرضی می باشد. پیش تیمار
سطحی را برای افزایش کارایی تجزیه ای و نیز تکرار پذیری آن ها انجام می دهند. معمولاً پیش تیمار از طریق صیقل دادن با استفاده از ذرات پودر
آلومینا به دست می آید. در این حالت الکترود باید با آب مقطر شسته و خشک شود و سپس مورد استفاده قرار گیرد.
الکترودهای الیاف کربنی
امروزه الیاف کربنی در تجزیه الکتروشیمیایی کاربرد وسیعی دارد. عمده ترین کاربرد آن ها در ساخت میکروالکترودها است. موادی با این چنین
استحکام بالا از طریق تجزیه حرارتی منسوجات پلیمری در دمای بالا از طریق لایه نشانی کاتالیزی بخار شیمیایی تهیه می شوند. این نوع الیاف
از طریق فرآیندهای ساخت متفاوتی تهیه شده و در اندازه های کوچک، متوسط و بزرگ کاربرد دارند.
الکترودهای الیاف کربنی از یک سری دسته های موازی رشته ای گرافیت ساخت شده اند. مزیت اصلی الکترودهای الیاف کربنی اندازه کوچک آن
ها می باشد (قطر ۵ تا ۳۰ میکرومتر برای الیاف کربنی تجاری) که در انواع محیط های با حجم کوچک، مانند تشخیص آزاد شدن انتقال دهنده های
عصبی در فضای بیرون سلول مغز مورد توجه قرار گرفته است.
الکترودهای خمیر کربن
الکترود خمیر کربن، در سال ۱۹۸۵ توسط آدامز ارائه شد. در حد فاصل سال های ۱۹۵۹ تا ۱۹۶۳ کاربرد الکترود خمیر توسط آدامز پیگیری شد. گروه
تحقیقاتی آدامز در فاصله این سال ها ویژگی های الکترود خمیر کربن را شناسایی و نحوه و ساخت و استفاده از آن را بررسی کردند.
الکترود خمیر کربن از مخلوط نمودن پودر کربن (گرافیت) و یک مایع خمیر کننده مناسب مانند پارافین به عنوان اتصال دهنده در یک بدنه الکترودی
استوانه ای و عایق که به شکل مناسب طراحی شده، قرار می گیرد. الکترود حاصل نیمه جامد بوده و قابلیت پولیش دادن را دارد. اندازه متداول
ذرات گرافیتی که در ساخت این الکترودها به کار می رود، بین ۲ تا ۵۰ میکرومتر می باشد. ذرات بزرگتر گرافیت خواص مکانیکی و الکتروشیمیایی
نا مطلوبی نشان می دهند.
قسمت رسانایی که در الکترود خمیر کربن به کار برده می شود (گرافیت)، باید خصوصیاتی نظیر اندازه مناسب ذرات (در حد میکرومتر)، توزیع
یکنواخت ذرات و درجه خلوص بالا را داشته باشد. بهتر است از به کارگیری پودرهای متخلخل و متنوع از نظر اندازه ذرات خودداری شود.
امروزه این نوع گرافیت از شرکت های تولید کننده مواد شیمیایی نظیر مرک، فلوکا و آلدریچ قابل خریداری می باشد. معمولاً قبل از استفاده از پودر
گرافیت هیچ آماده سازی بر روی آن انجام نمی شود. در ضمن اگر گرافیت نرم و پودری نباشد، موجب ناهمواری سطح الکترود و کاهش تکرار
پذیری آن می شود. بنابراین استفاده از گرافیت با خلوص بالا، دانه بندی بسیار ریز و پودری حائز اهمیت است.
جزء دیگر خمیر کربن، مایع نگهدارنده است. از معمولی ترین آن ها روغن پارافین و نوجول می باشند. این مایعات چسبنده، غیر قطبی و نارسانا
(عایق) تمامی خواص مهم یک اتصال دهنده خوب را دارا می باشند.
یک اتصال دهنده خوب باید دارای ویژگی های زیر باشد :
– از نظر شیمیایی تا حد امکان بی اثر;
– دارای فراریت کم ;
– غیر قابل امتزاج با محلول مواد مورد اندازه گیری (آبی) ;
– ویسکوزیته و پایداری مناسب در مخلوط خمیر کربن;
– عاری از ناخالصی ها;
– بی اثر بودن بر محلول های آبی از نظر شیمیایی و الکتروشیمیایی
مایع خمیر کربن نه تنها ذرات گرافیت را به هم می چسباند، بلکه آن ها را از محلول آبی محافظت می کند و باعث هیدروفوبیک کردن سطح
الکترود می شود. در حقیقت افزایش خصلت چربی دوستی (آبگریزی) مایع خمیر کننده، مانع دسترسی گونه آبدوست مورد اندازه گیری به سطح
الکترود می شود. به طور کلی وجود مایع نگهدارنده در سطح الکترود سرعت انتقال الکترون را کاهش می دهد.
نسبت دقیقی بین مقادیر پودر گرافیت و مایع نگهدارنده برای تهیه خمیر کربن گزارش نشده است.
اگر مقدار مایع نگهدارنده جهت تهیه خمیر کربن زیاد باشد، خواص سینتیکی و الکتریکی الکترود نامطلوب شده و اگر مقدار آن کم باشد، خمیر
کربن حاصل خشک بوده و تجدید پذیری سطح آن دشوار می شود و در نتیجه تکرار پذیری آن کاهش می یابد.
برای آماده سازی خمیر کربن، انتخاب مناسب اجزای سازنده و نسبت آن ها موارد سودمندی است که بررسی شده است. این بررسی نشان
می دهد که روش های دستی سنتی همگن کردن خمیر در هاون هنوز ترجیح داده می شود.
مخلوط های خمیر آماده برای استفاده به صورتتجاری موجود می باشند.
از مزایای آماده کردن خمیر توسط تجزیه گر در آزمایشگاه می توان به انتخاب اجزای سازنده آن و تعیین نسبت متقابل آن ها اشاره کرد. البته
دست ساز بودن خمیر کربن برای ساختن خمیر کربن اصلاح شده تقریباً اجتناب ناپذیر می باشد.
در واقع خصوصیتی که یک الکترود خمیر کربن از خود نشان می دهد از انتخاب اجزاء خمیر، کیفیت، نسبت اجزاء و همچنین راه تهیه و همگن
سازی خمیر ناشی می شود.
خمیر کربن تهیه شده را می توان داخل لوله های شیشه ای، کوارتزی و تفلونی با قطرهای متفاوت و هم درون نگهدارنده های الکترودی
مخصوص قرار داد. متداولترین نوع نگهدارنده های الکترودی، ساختاری پیستونی شکل دارند که به راحتی خروج کربن را از سوراخ انتهای الکترود
امکان پذیر می سازند.
معمولاً این قسمت از الکترود را از ماده شیمیایی غیر فعال می سازند.
در سال ۱۹۶۴ به دلیل ساختار ترکیبی خمیر کربن و تهیه آسان آن، مجدداً آدامز به این فکر افتاد که برای بهبود بخشیدن یا تغییر دادن خواص
الکترود به منظور اهداف مطالعاتی، مواد دیگری به غیر از دو جزء اصلی خمیر کربن به خمیر الکترود اضافه کند.
اولین گزارش تهیه الکترود خمیرکربن اصلاح شده توسط کاوانا و فرنچ در سال ۱۹۷۴ در آزمایشگاه آدامز ارائه شده.
آن ها نشان دادند که خمیر کربن می تواند اجزای دیگری نیز داشته باشد که به طور آشکار رفتار کلی الکترود را تغییر می دهد. آن ها اولین قدم را
برای تهیه و توسعه الکترودهای خمیر کربن اصلاح شده برداشتند.
اولین کاربرد الکترودهای خمیر کربن اصلاح شده توسط چک و نلسون با وارد کردن گروه های عاملی کمپلکس دهنده در سطح الکترود به منظور
پیش تغلیظ نقره انجام پذیرفت.
اما اولین پیشرفت چشمگیر در استفاده از الکترودهای خمیر کربن توسط بالدوین و همکارانش ارائه شده.
او پیشنهاد نمود که مخلوط کردن مستقیم خمیر کربن با عامل اصلاح گر می تواند راهی مناسب و ساده برای تهیه الکترود خمیر کربن اصلاح
شده باشد.
در الکترودهای اصلاح شده، عامل اصلاح گر با کاهش حد تشخیص و افزایش گزینش پذیری برای برخی گونه های مورد اندازه گیری سبب بهبود
کارایی، انتخابگری و حساسیت الکترود می شود.
اصلاح الکترودها به منظور استفاده در کاربردهای تجزیه ای، توجه الکتروشیمیدان ها را به خود جلب کرده است.
اصلاح گر باید در محلول تجزیه ای غیر قابل حل باشد و جذب قوی با ترکیبات خمیر داشته باشد ، تا از حل مولکول های موجود در سطح الکترود در
طی اندازه گیری جلوگیری کند.
برای به دست آوردن نتایج تکرار پذیر، غلظت ترکیبات موجود بر روی سطح الکترود در طی آزمایشات یکسان باشد.